2020年2月26日,国际著名学术期刊《先进功能材料》在线发表了生物电子学国家重点实验室梁高林教授课题组和吴富根教授课题组的合作研究成果,文章标题为《Enzyme-Mediated Tumor Starvation and Phototherapy Enhance Mild-Temperature Photothermal Therapy》。该文章报导了一种酶介导的肿瘤饥饿和光疗的策略,在增强肿瘤的低温光热治疗效率方面取得重要进展(Adv. Funct. Mater., 2020, 1909391)。
光热疗法(PTT)利用激光照射下所产生的高热(高于45 oC)来破坏癌细胞,已经逐步成为用于癌症治疗的重要手段。然而,高热可能会导致健康组织损伤,肿瘤转移和复发等问题。因此,温和PTT的采用(温度低于45 oC)可以在避免副作用的情况下实现对肿瘤的治疗,但在实体瘤内实现最大限度增强温和PTT效率同时避免副作用的策略尚未见报道。梁高林教授课题组和吴富根教授课题组合理地设计出一种多功能温度敏感型脂质体,通过脂质分子DPPC和DSPE-PEG2000制备了温敏相转变脂质体,以封装葡萄糖氧化酶(GOx),吲哚菁绿(ICG)和藤黄酸(GA),所形成的载药温敏脂质体GOIGLs实现了这些药物在肿瘤部位的热响应递送和低温热疗(见下图1)。具体来说,NIR激光可以触发GOIGLs中所载的ICG的光热效应。达到42 oC后,GOIGLs经历了从凝胶相到液晶相的转变,导致加载的GA和GOx等组分从脂质体中快速释放。一方面,释放的GA可以在NIR激光照射下从溶酶体逃逸到细胞质中。然后,GA与热疗引起的过表达的热休克蛋白90(HSP90)进一步结合并抑制其活性,从而克服了癌细胞的耐热性并实现了温和的PTT。另一方面,释放的GOx有效地催化了葡萄糖的氧化和过氧化氢的产生。葡萄糖的消耗导致能量的供应受到限制,从而抑制了HSP90,进而提高了温和肿瘤PTT的效率。而且,在450‒750 nm光照射下,生成的过氧化氢转化为•OH(羟基自由基),有效破坏了癌细胞,实现了对肿瘤的酶增强的光热作用。细胞和动物实验结果均表明,这一肿瘤饥饿和光疗策略显着提高了温和PTT对肿瘤的治疗效率。该策略为解决低温光热效率和用药剂量之间的矛盾提供了一种可行且可靠的手段。更重要的是,通过用酶介导的肿瘤饥饿和光疗来增强低温光热治疗效率,这种“智能”策略有望加速光热治疗的临床转化。
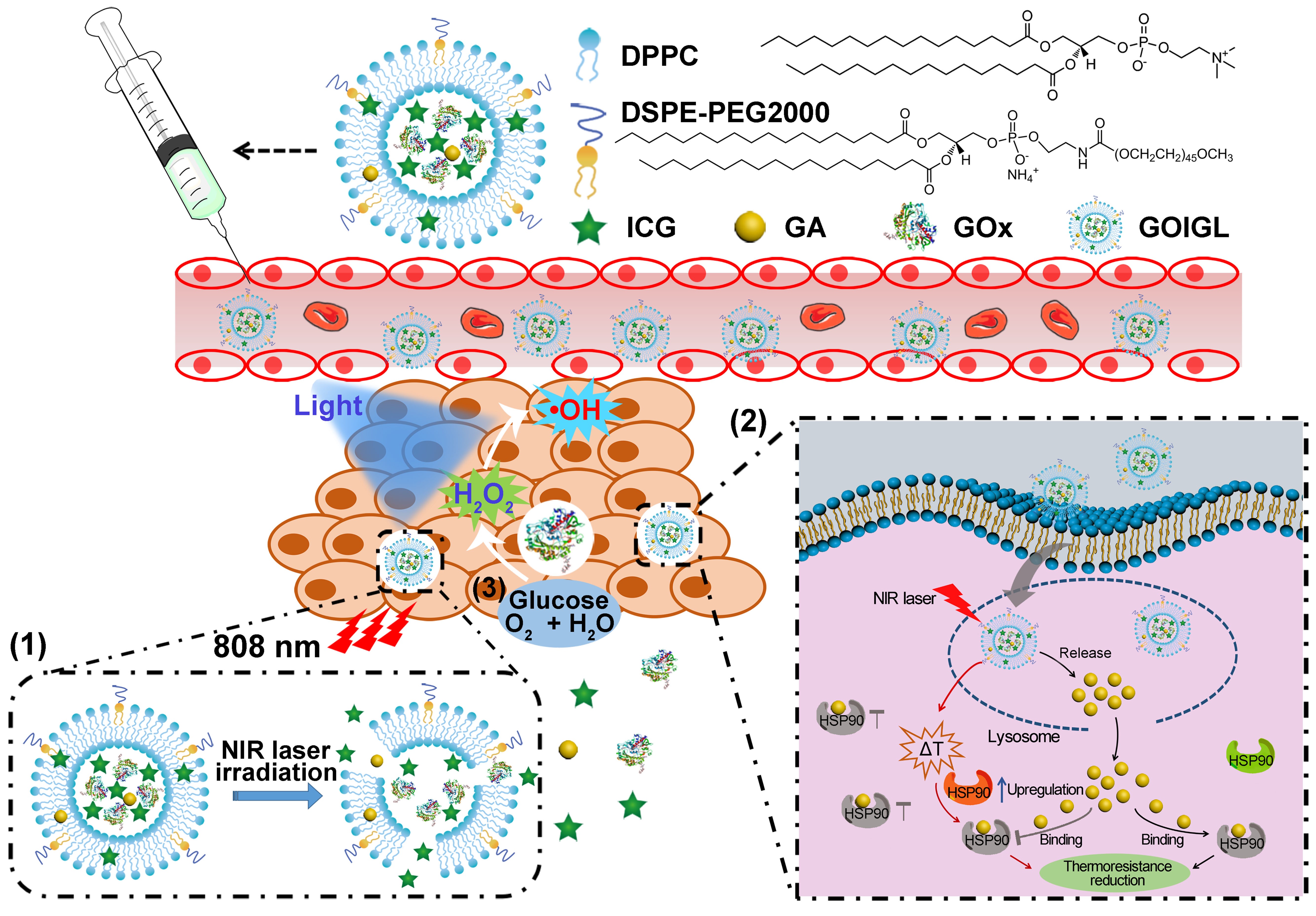
图1:肿瘤饥饿疗法、酶增强光疗和低温热疗协调作用示意图。
该论文的第一作者为东南大学生物科学与医学工程学院博士生高歌。梁高林教授和吴富根教授为共同通讯作者。
该项目研究得到了国家自然科学基金以及国家重点研发计划的资助。
(生物电子学国家重点实验室)
附文章链接:https://doi.org/10.1002/adfm.201909391




