肝癌是全球重要的健康挑战,也是中国最常见的癌种之一,其发病率和死亡率居高不下。由于晚期发现率高、早期筛查不足、治疗手段有限等,中国肝癌患者的五年生存率较低。目前肝癌的主要治疗手段包括手术、局部消融、肝移植、靶向治疗和免疫疗法等。但大多数患者确诊时已处于晚期或伴随严重肝硬化,手术和肝移植适用范围有限。靶向治疗和免疫治疗虽为晚期患者提供了新选择,但因肝癌分子异质性高,疗效差异大且整体获益有限。因此,针对肝癌患者的个性化治疗显得尤为重要。通过基因组学分析和体外药物敏感性测试来制定特异性治疗方案,提高疗效和生存率,已成为亟待解决的临床问题。
近日,东南大学数字医学工程全国重点实验室顾忠泽教授团队,与南京医科大学第一附属医院肝胆中心成峰教授团队,东南大学生命科学与技术学院李健教授等团队合作,在International Journal of Biological Sciences发表研究成果“Leveraging Patient-Derived Organoids for Personalized Liver Cancer Treatment”。
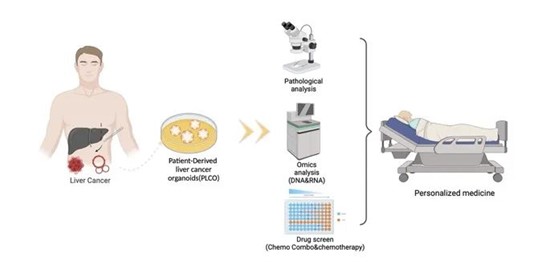
本研究成功构建了患者来源的肝癌类器官(PLCOs)体外模型,并通过改良培养方法和高效筛查流程,大幅提高了肝癌类器官的生成效率和成功率,并使类器官保留了与原始肿瘤一致的突变和遗传特征。通过药物敏感性筛查,PLCOs能够准确预测患者特异性的药物反应,为个性化治疗提供了直接依据。结果显示,类器官在药物测试中的患者特异性反应与临床治疗效果相符,进一步验证了其作为预临床筛查模型的潜力,为未来肝癌个性化药物开发和治疗方案的选择提供了新的工具和临床支持。
1
类器官的建立及组织病理学评估
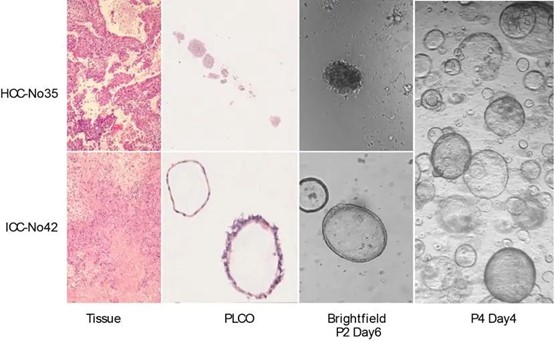
本研究首先对成功培养的PLCOs进行组织病理学评价,发现这些类器官能较好地保留原始肿瘤组织的结构特征。例如,HCC的类器官形成了类似肝索和假腺管型结构,而ICC的类器官则呈现出腔样结构。H&E染色结果显示,PLCOs与原始肿瘤在组织形态上具有高度一致性,展示了其在长期培养(最长可达3个月)中的稳定性和紧密结构。这些类器官不仅保留了肿瘤的基本结构,还在形态上展示了肿瘤亚型的特异性特征。
2
PLCO对基因组变化的重现
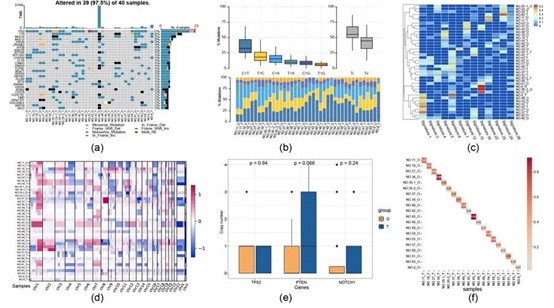
突变分析显示在一些配对的肿瘤和类器官中,突变型转换(Ti)和颠换(Tv)的比例保持了很好的一致性。20 对配对的肿瘤与类器官中,有 12 对的拷贝数一致性超过 30%,本研究43 号和 34 号病人的类器官肿瘤拷贝数的一致性则分别高达92%和86%。
3
PLCO对表达谱的重现

转录组分析表明,类器官和肿瘤组织的转录组在整体上存在差异,但同时也保持了一定的个体特异性,而肿瘤组织与对应的PLCO之间的表达则较为一致。进一步分析差异表达基因发现,类器官基本保留了肿瘤组织中癌细胞的转录组特征,主要差异来自于类器官缺乏免疫微环境。
随后,研究通过单细胞分析提取癌细胞的特征基因,并比较其在多批类器官和癌细胞系中的表达模式。定量对比结果显示,本研究构建的PLCO比传统癌细胞系更能保留癌细胞的特征。此外,本研究培养的PLCO在转录特征上比大多数已发表的PLC类器官更接近真实癌细胞。
4
PLCO识别患者特异性的药物敏感性
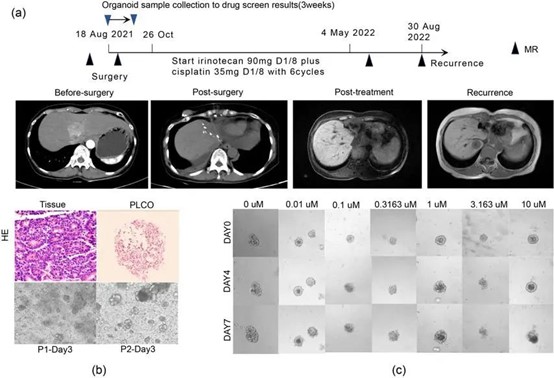
随后,本研究利用类器官检测了临床常用的肝癌相关药物或化疗方案的敏感性。研究中采用了优化的类器官培养模式,并且在培养过程中采用深度学习的方法快速量化和计算消化类器官的数量和直径参数,减少了人为干预并提供更准确的测量结果。结果提示类器官对特定病人不同治疗方案的反应有明显差异。以43号病人为例,该病人是一位60岁胆管癌复发患者,其衍生类器官的药物敏感性预测其对伊立替康联合顺铂敏感,随后患者接受该方案的辅助化疗,治疗效果良好。这一研究验证了PLCOs在个体化用药选择中的潜力,有望用于精确指导肝癌患者的个性化治疗。
南京医科大学第一附属医院肝胆中心饶建华副教授,东南大学数字医学工程全国重点实验室宋超博士、陈早早教授,东南大学生命科学与技术学院郝阳阳博士,为共同第一作者。该论文得到了江苏省自然科学基金重大项目、国家自然科学基金和江苏省人民医院(南京医科大学第一附属医院)临床能力提升项目的资助。
原文链接:https://www.ijbs.com/v20p5363.htm




